厚労省がMerck社のモルヌピラビルを特例承認、初のCOVID-19経口薬
厚労省がMerck社のモルヌピラビルを特例承認、初のCOVID-19経口薬
厚生労働省は2021年12月24日、新型コロナウイルス感染症(COVID-19)治療薬として承認申請されていた「ラゲブリオ」(モルヌピラビル)について、特例承認した。同日開催された薬事・食品衛生審議会医薬品第二部会で承認が了承されたことを受けての措置。軽症から中等症IのCOVID-19患者に使用できる経
国際共同第3相試験のデータで、入院または死亡に至った被験者の割合が、モルヌピラビル群で7.3%(28/385例)、プラセボ群で14.1%(53/377例)となり、リスク減少率は48%で統計学的に有意な差が認められた。ただし、全ての被験者を対象とした解析では、モルヌピラビル群で6.8%(48/709例)、プラセボ群で9.7%(68/699例)となり、リスク減少率は30%に低下した。
この点について、米Pfizer社の「PAXLOVID(パクスロビド)」 (nirmatrelvir+ritonavir)は臨床試験で89%のリスク減少率が達成されており、単純比較はできないものの、モルヌピラビルの有効性が見劣りする状態となっている。
なんだか、超短命が約束されているような薬剤といったら失礼か?
モルヌピラビルは“妊娠”が問題となりそう
一方、パクスロビドはeGFRにて用量設定必要 eGFR<30では使用できない。妊娠・授乳に関してはデータ不足というスタンス
Paxlovid (nirmatrelvir/ritonavir) dosing, indications, interactions, adverse effects, and more
Medscape - COVID-19 disease dosing for (Paxlovid) nirmatrelvir/ritonavir, frequency-based adverse effects, comprehensive interactions, contraindications, pregna...
1
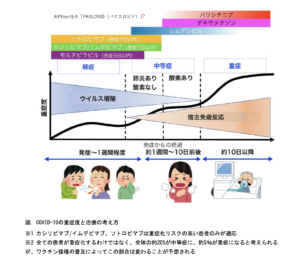
COVID-19 に対する薬物治療の考え方 第 11 版
(2021年12月24日)
https://www.kansensho.or.jp/uploads/files/topics/2019ncov/covid19_drug_211224.pdf


